Termodinâmica: resumo com fórmulas
A Termodinâmica é a parte da Física que estuda a transformação de energia térmica em trabalho. Entenda aqui, com fórmulas
A Termodinâmica é a parte da Física que estuda principalmente a transformação de energia térmica em trabalho.
A utilização direta desses princípios em motores de combustão interna ou externa, faz dela uma importante teoria para os motores de carros, caminhões e tratores, nas turbinas com aplicação em aviões, etc.
1. Trabalho em uma Transformação Isobárica
A transformação isobárica, como o nome diz, é uma transformação em que variam somente o volume e a temperatura de um gás, sendo a pressão mantida constante.
Nesse caso o trabalho realizado pode ser expresso por:

Caso haja uma expansão (aumento de volume) o trabalho será positivo; em caso contrário, numa contração do gás, o trabalho será negativo.
2. Energia Interna dos Gases
Um gás que possua uma temperatura diferente do zero absoluto (0 K) possui uma energia cinética interna representada pela energia cinética de suas partículas em movimento:

3. Primeiro Princípio da Termodinâmica
“Se um sistema gasoso recebe energia na forma de calor externo (Q), essa energia pode ser armazenada ou pode se transformar em trabalho”.
A variação de energia interna pode ser expressa por:

Para as diferentes transformações o resumo da Primeira Lei da Termodinâmica seria:
3.1. Transformação isotérmica (sem variação de temperatura)
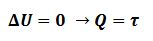
Ou seja, na transformação isotérmica todo calor cedido pelo meio é transformado em trabalho de expansão do gás e, mesmo não havendo variação de temperatura, há troca de calor com o meio externo.
3.2. Transformação isobárica (sem variação de pressão)
O calor externo será:
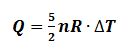
3.3. Transformação isocórica (sem variação de volume)
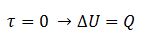
3.4. Transformação adiabática (sem troca de calor com o ambiente externo)
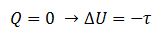
4. Teorema de Carnot
Uma máquina térmica, para funcionar de maneira contínua, deve receber o calor de uma fonte quente (Q1) a uma certa temperatura (T1), transformar parte dessa energia em trabalho e devolver o restante (Q2) para uma fonte fria a uma temperatura (T2), sendo que (T2
O rendimento dessa máquina será:
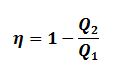
Com as energias térmicas em módulo.
E, segundo o Teorema de Carnot, o rendimento máximo de uma máquina térmica será:

Obs.: nas máquinas frigoríficas a definição acima ficará:
Na máquina térmica frigorífica, a intenção é utilizar uma fonte de energia mecânica externa, por exemplo, um motor elétrico, para transferir calor de uma fonte de menor temperatura para uma de maior temperatura.
| Exercícios |
| 1. (Vunesp-SP) A energia interna U de uma certa quantidade de gás, que se comporta como gás ideal, contida em um recipiente, é proporcional à temperatura T, e seu valor pode ser calculado utilizando a expressão U=12,5T. A temperatura deve ser expressa em kelvin e a energia, em joules. Se inicialmente o gás está à temperatura T =300 K e, em uma transformação a volume constante, recebe 1 250 J de uma fonte de calor, sua temperatura final será:
a) 200 K |
| 2. (Mackenzie-SP) Um gás, contido em um recipiente dotado de um êmbolo que pode se mover, sofre uma transformação. Nessa transformação fornecemos 800 cal ao gás e ele realiza o trabalho de 209 J. Sendo 1 cal=4,18 J, o aumento da energia interna desse gás foi de: a) 209 J |
| 3. (Uema) Sobre um sistema realiza-se um trabalho de 3 000 J e, em resposta, ele fornece 500 cal de calor durante o mesmo intervalo de tempo. A variação de energia interna do sistema durante esse processo é: (Dado: 1 cal =4,2 J.) a) 2 500 J |
Respostas:
1. c
2. b
3. c






















