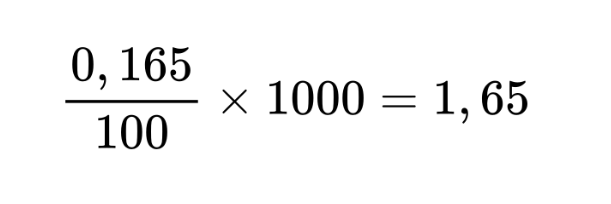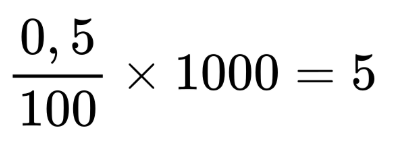Resumo de Química: Densidade, concentração e molaridade
O que é preciso saber para o vestibular
Destes três conceitos que são relativamente próximos, há de se fazer uma diferenciação: a densidade é o único destes que é uma propriedade intrínseca da matéria, lembrando que a matéria tem duas características fundamentais: possui massa e ocupa lugar no espaço.
Densidade
A relação entre a massa e o volume de um corpo qualquer recebe o nome de densidade, que pode ser matematicamente expressa como:
d = m / v
Concentração
Já a concentração se refere sempre a uma solução que contem pelo menos dois componentes: soluto e solvente. Soluto é aquele que está dissolvido, solvente aquele que dissolve.
A concentração nada mais é do que a relação entre a massa do soluto (o que está dissolvido) e do volume da solução.
Molaridade e concentração molar
Em Química as quantidades são, quase sempre, expressas em mols ou moles (plural de mol). É a partir dai que se pode calcular a concentração molar. Chamamos de concentração porque ela está sempre relacionada à quantidade de soluto por volume e molar porque essa quantidade não será expressa em quantidade de massa, mas sim em moles.
A molaridade nada mais é então que a relação entre a quantidade de soluto expressa em moles e o volume da solução.
M = n / v